隨著最近埃博拉和新冠病毒產品的批準,腺病毒載體已成為一類重要的疫苗。在腺病毒載體制造過程中收集的過程質量屬性數據主要集中在顆粒濃度和感染性比例(基于病毒基因組:針對細胞的感染性),數據表明最終疫苗產品中只有一小部分病毒顆粒是有效的。為了更好地了解這種產品的異質性,使用透射電鏡 (TEM) 研究了兩種腺病毒載體 (黑猩猩腺病毒(ChAdOx1) 和人類腺病毒5型 (Ad5)) 的實驗室規模制備。對不同的腺病毒形態進行了表征,并對空顆粒和完整顆粒的比例進行了量化。這些比例與樣品的感染性值表現出定性的相關性。采用液相色譜-質譜 (LC-MS) 多肽圖譜鑒定參與病毒成熟的關鍵腺病毒蛋白。利用肽豐度分析,從ChAdOx1病毒CsCl超速離心制備的低 (空) 和高密度 (完整) 組分中觀察到L1 52/55k豐度的變化約為5倍。L1 52/55k病毒蛋白與DNA包裝有關,并在病毒成熟過程中被切割,因此它可能是感染顆粒的標記物。作為腺病毒載體過程監測的一部分,TEM和LC-MS肽圖譜是極有應用前景的高分辨率分析表征工具,可以幫助區分空的、非感染性的和感染性病毒顆粒的相對比例,這些結果是一個鼓舞人心的開發進程的第一步,可以更好地區分不同的產品相關雜質。
腺病毒載體有許多治療和預防用途,包括商業化基因治療產品和疫苗。它們是一類重要的病毒載體,因為它們可以遞送大量核酸有效負載 (8-36 kbp),因此可以實現需要遞送大量核酸的治療性轉座子有效載荷進入目標基因組。腺病毒是第一個進入嚴格治療開發的 DNA 病毒,因為它具有明確的生物學特性、遺傳穩定性、高基因轉導效率,且相對容易大規模生產。由于保質期長,它們是很有吸引力的候選疫苗平臺,且通過使用不同的添加物和制劑策略,可以進一步延長保質期。
有許多檢測方法和技術可用于根據監管指南來表征腺病毒的不同結構屬性。當前基于病毒載體的疫苗的質量控制檢測方法包括:通過 PCR 進行的顆粒計數、顆粒與感染率的比例(確定通過基于細胞的感染性測定),殘留宿主細胞 DNA 和殘留宿主細胞蛋白。在這項工作中,我們評估了更高分辨率結構分析的潛在效用,包括液相色譜-質譜法 (LC-MS) 和透射電子顯微鏡 (TEM) 作為在基于腺病毒的疫苗的工藝開發過程中使用的分析表征工具。這些分析工具提供了更大程度的“互補”產品理解,TEM 提供了病毒顆粒形態的證據,LCMS 允許測量病毒蛋白質組。
黑猩猩腺病毒 (ChAdOx1) 和人類腺病毒 5 型 (Ad5) 這兩種通常用于商業生產的載體在本研究中進行了表征。兩種病毒載體均通過氯化銫密度梯度超速離心分離,另外對于 Ad5,還使用了陰離子交換膜層析,以評估純化腺病毒的異質性。腺病毒生產的問題之一是存在與產品相關的雜質,例如空的和未成熟的(非感染性顆粒)。雖然目前使用的檢測方法描述了它們的存在和比例,但它們沒有提供可用于闡釋其存在的根本原因的信息,而這將有利于在生產過程中合理地設計它們。目前正在進行腺相關病毒 (AAV) 領域的研究,以增加針對 AAV 的哪些特征與效力有關的理解。最近,利用高分辨率天然質譜法研究了幾種AAV血清型的組成,發現了具有不同衣殼組成的高度異質性的群體。
腺病毒中的產品相關雜質可能來自病毒顆粒成熟周期的不同階段,其經歷了一系列結構變化(圖 1)。這些結構變化由參與衣殼組裝、DNA 包裝和顆粒成熟的關鍵腺病毒蛋白控制。關鍵的腺病毒蛋白及其功能列于表 1 中,作為成熟過程的一部分,許多這些腺病毒蛋白會進行蛋白水解切割。此外,錯誤包裝和蛋白水解裂解可能會產生與產品相關的雜質;空的病毒顆粒可能是在成熟前收獲導致的,或者可能是包裝過程中由于某些因素阻止成熟而導致的錯誤結果。成熟過程的時間順序有許多方面仍未完全了解。
腺病毒殼蛋白 IA、VF 和 VIII 以及核心蛋白 VII、pl 和 TP 作為前體合成,并在組裝過程中由腺病毒蛋白酶 (AVP) 加工。定量蛋白質組學研究顯示了 AVP 拷貝數,每個病毒顆粒只有7個 AVP 分子。每個病毒顆粒大約需要發生 2000 次切割,導致每個 AVP 拷貝發生約 40 到 300 次切割。這些切割必須在病毒核高度擁擠的環境中發生,因為它們與病毒DNA相互作用。包裝支架 L1 52/55k 蛋白預計會被 AVP 切割。未成熟顆粒含有約 50 個全長 L1 52/55k 拷貝,而成熟病毒顆粒中不存在該蛋白。
因此,這些病毒蛋白是腺病毒成熟的潛在指示標志物,可以通過 LC-MS 觀察以監測各種 Ad5 顆粒的結構和比例。由于某些表面病毒蛋白的拷貝數較低,因此可能難以通過 LC-MS 進行鑒定。此外,顆粒經歷的結構變化可能會導致形態學變化,這些變化可以使用 TEM 觀察到。最終,這兩種方法可能會用于檢測 Ad5 產品雜質和工藝開發的異質性,并且所識別的標記蛋白可能會用于質量控制、GMP 背景中基于 ELISA 的分析的基礎。
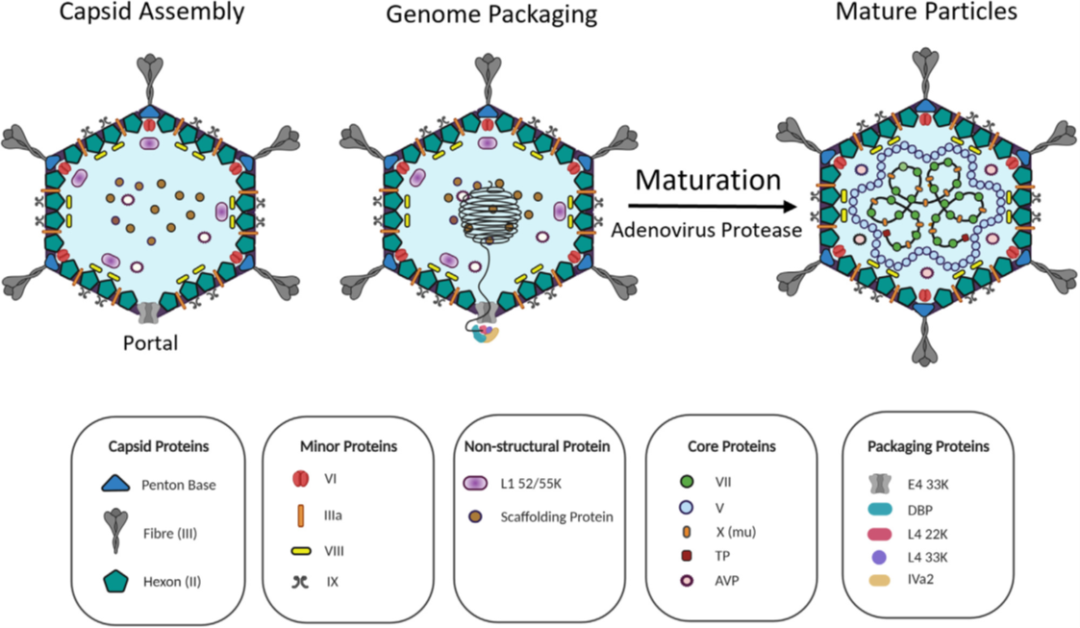
圖1. 腺病毒顆粒形成和成熟過程的示意圖。衣殼首先由一個頂點作為入口組裝。包裝蛋白與入口頂點和病毒DNA結合,將DNA運送到組裝好的衣殼中。成熟為感染性腺病毒顆粒是通過腺病毒蛋白酶(AVP)裂解關鍵的腺病毒蛋白和病毒DNA的凝聚而發生的。
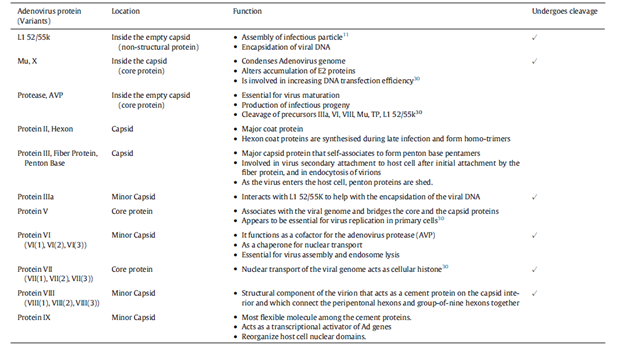
表1. 關鍵的腺病毒結構蛋白及其功能特性。
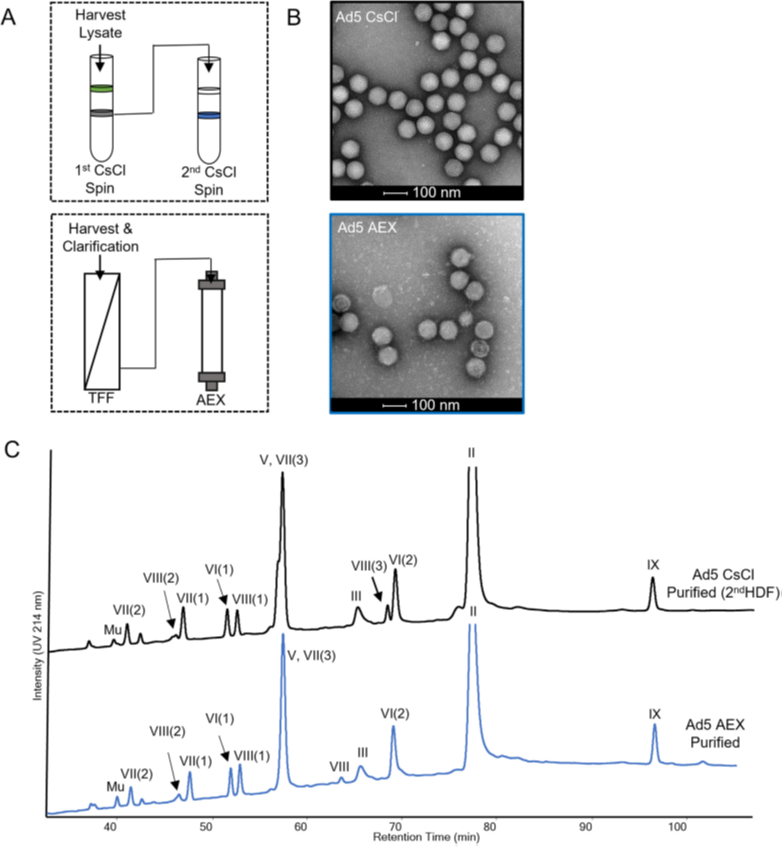
圖2. CsCl超速離心或TFF-AEX純化過程中Ad5樣品的外觀和組成的表征。(A) Ad5餾分的純化流程圖。(B) Ad5樣品的代表性TEM顯微圖,Ad5樣品取自第二次CsCl離心的高密度餾分和AEX洗脫液 (100 nm標尺)。(C) CsCI (黑色)或AEX(藍色) 純化Ad5的代表性RP-UHPLC圖譜。通過LC-MS肽圖鑒定每個峰的Ad5蛋白。
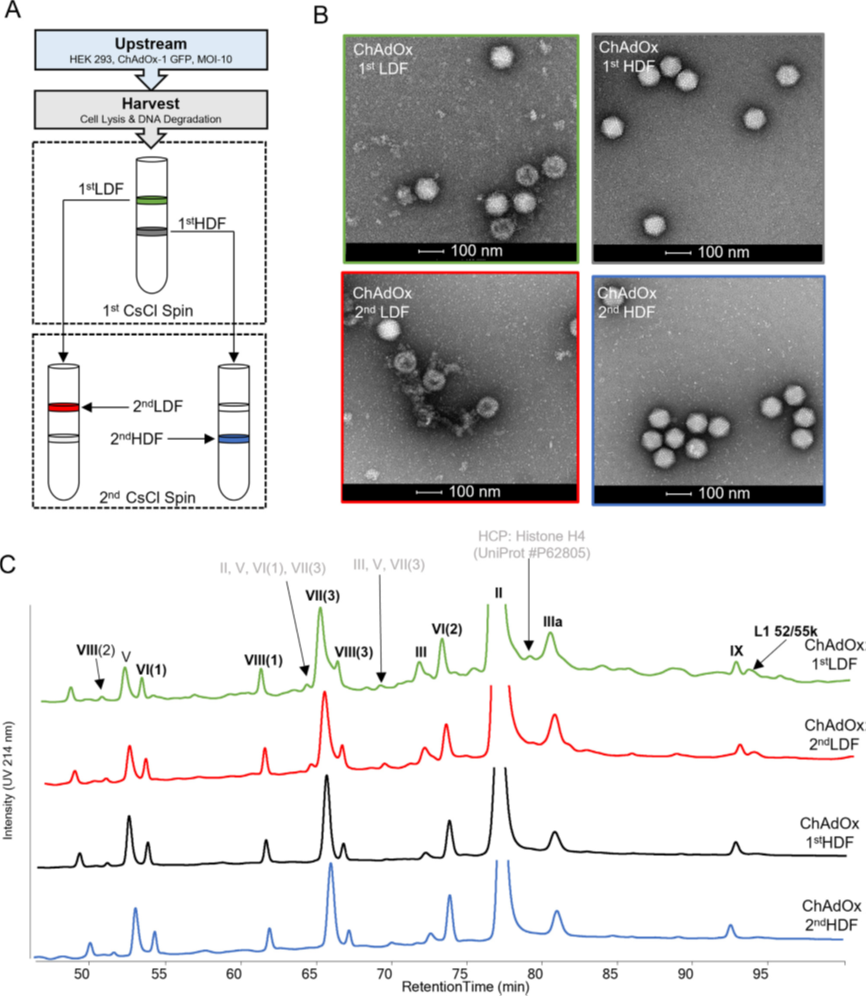
圖3. CsCl純化過程中ChAdOx1-GFP樣品的外觀和組成表征。(A) ChAdOx1-GFP餾分流程圖。(B) 第一或第二個CsCl純化步驟的 LDF或HDF ChAdOx1-GFP的代表性TEM顯微圖 (100 nm標尺)。(C) CsCl純化ChAdOx1-GFP的代表性RP-UHPLC圖譜。第一或第二個CsCl離心步驟的低密度部分(LDF) 分別以綠色或紅色顯示,而第一或第二CsCl步驟的高密度部分 (HDF) 分別以黑色或藍色顯示。
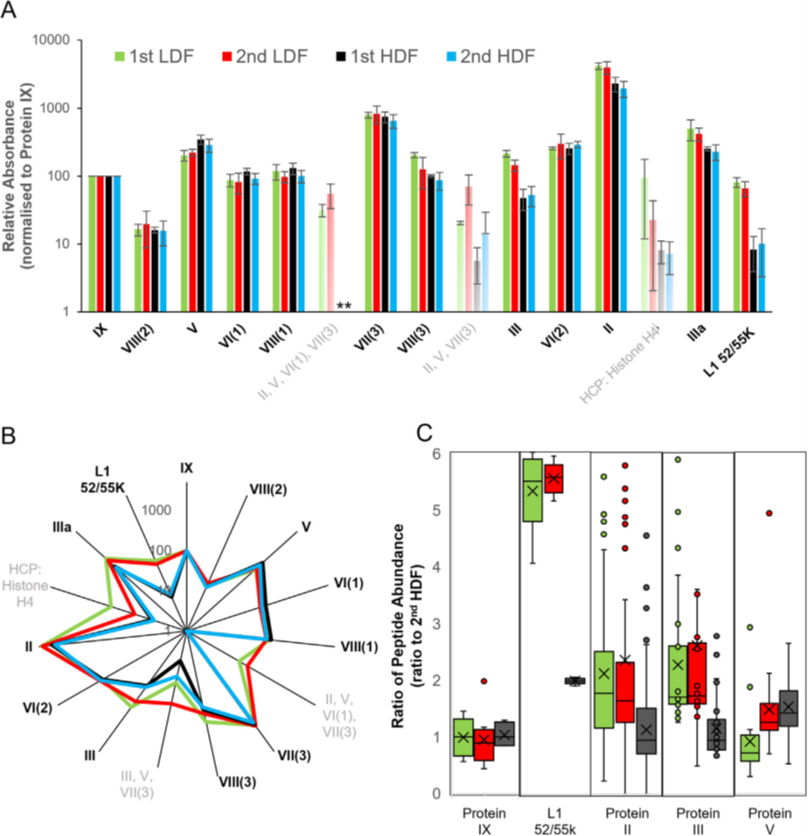
圖4. 純化過程中ChAdOx1-GFP樣品LC-MS肽圖譜數據集相對蛋白質定量方法的比較。(A)不同ChAdOx1-GFP CsCl組分的相對RP-UHPLC峰比較。各CsCl組分的RP-UHPLC峰豐度歸一化為Protein IX峰。誤差條表示三次重復的MS測量。星號(*)表示在HDF樣本中未觀察到的峰值。(B) 圖(A)中相同數據集的可視化雷達圖。灰色表示的蛋白質低于定量限制。(C) ChAdOx1-GFP CsCl餾分中代表性病毒蛋白的相對肽豐度與第二高密度餾分的兩兩比較。
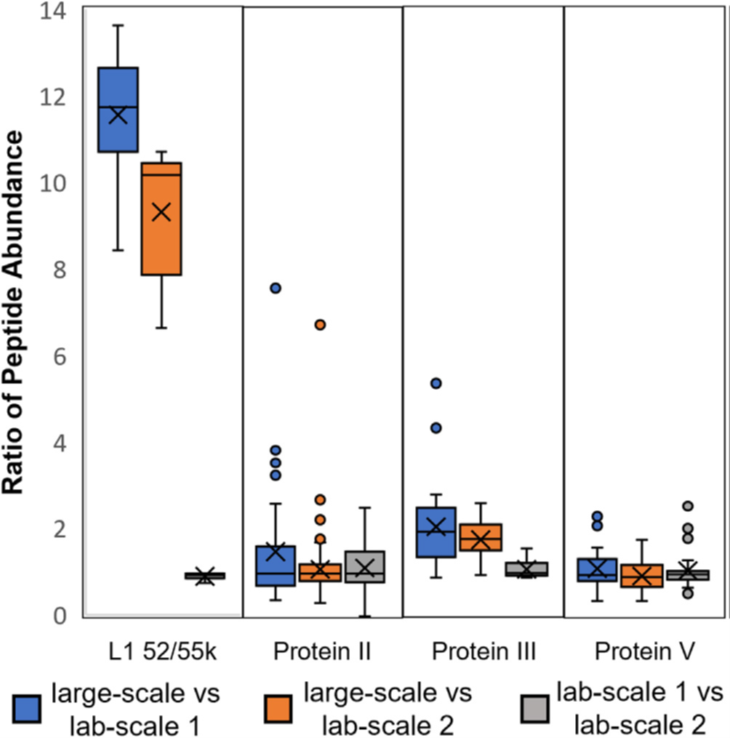
圖5. ChAdOx1 nCoV-19肽分析。分析的樣品取自一種大規模AEX制劑和兩種不同P:l比的實驗室規模CsCl制劑,并對四種不同病毒蛋白的肽豐度比進行兩兩比較。圖中顯示了3種不同的比較:藍框-大規模AEX (病毒顆粒:感染性病毒顆粒(P:I)比為97)和實驗室規模 CsCl 1 (P:I比為68);橙框-大規模AEX (P: 1比97)和實驗室規模CsCl 2 (P: 1比31);灰框-實驗室規模CsCl 1 (P:I比例為68)和實驗室規模CsCl 2 (P:I比例為31)。
總結
在這項研究中,評估了兩種更高分辨率的分析技術,作為在工藝開發過程中表征腺病毒載體質量的潛在工具。首先,人腺病毒血清型 5 (Ad5) TEM 分析表明,在通過 CsCl 超速離心(95% 完整顆粒,P:I 比例 4)或 AEX 層析制備的樣品中,更高豐度的完整顆粒與更高(更低)的感染率相關(76% 的完整顆粒,P:I 比例 14)。這種相關性在 CsCl 超速離心制備的 ChAdOx1-GFP 樣品中得到證實,樣品取自第 1 和第 2 個 LDF(62/45%,P:I 比例 113/77)和第 1 和第 2 個 HDF(93/99%,P:I 比例 79/56)。其次,ChAdOx1-GFP LC-MS 肽圖分析還證明了感染率與特定讀數(L1 52/55k 的相對豐度)之間的相關性,包括 LDF(5.5/5.6,P:I 比例 113/77) 和 HDF (2.0/1.0, P:I 比例 79/56) 的載體樣本。使用通過 CsCl 超速離心或 AEX 層析純化的 ChAdOx1 載體 (ChAdOx1 nCoV-19) 進一步評估了 LC-MS 肽圖分析方法的效用,觀察到與 CsCl 樣品(P:I 比例為 68 和 31)相比, 在 AEX 樣品中(P:I 比例 97)的L1 52/55k 的相對豐度有 10 到 12 倍的差異。總而言之,這項工作中提供的數據顯示了通過 TEM 圖像分析確定的不完整載體顆粒的比例以及通過 LC-MS 肽豐度分析確定的 L1 52/55K 豐度與使用更標準的基于細胞的技術測量的感染率相關,例如,與 LDF 相比,HDF 樣品顯示出較低豐度的空(不完整)顆粒和蛋白質 L1 52/55k。雖然呈現的結果是令人鼓舞的第一步,但 TEM 和 LC-MS 肽圖分析技術都有可能提供更多關于腺病毒載體樣品質量的、數據豐富的數據集,并證明它們作為工藝開發工具的價值。鑒于基于腺病毒的載體的重要性,使用更高分辨率的分析工具更好地了解生產過程及其對產品質量/感染性的影響對于提高生產一致性和降低成本至關重要。
原文:J.M.Hicky, S.I.Jacob, A.S.Tait, et al., Measurement of Adenovirus-based Vector Heterogeneity, Journal of Pharmaceutical Sciences, 2023.






