根據研討會期間收集的信息,參與者指出的實施連續生物工藝HTPD的主要挑戰列于表 2。此外,參與者針對所討論的每個挑戰提出了可能的解決方案。建模和微/納米流體是這些領域進一步投資/優先考慮的主要建議,以便更輕松、更順利地過渡到連續生物生產。這些提議的解決方案和 ICB 中的其它當前需求將被進一步討論,特別關注 PAT 工具和單元操作的連接。
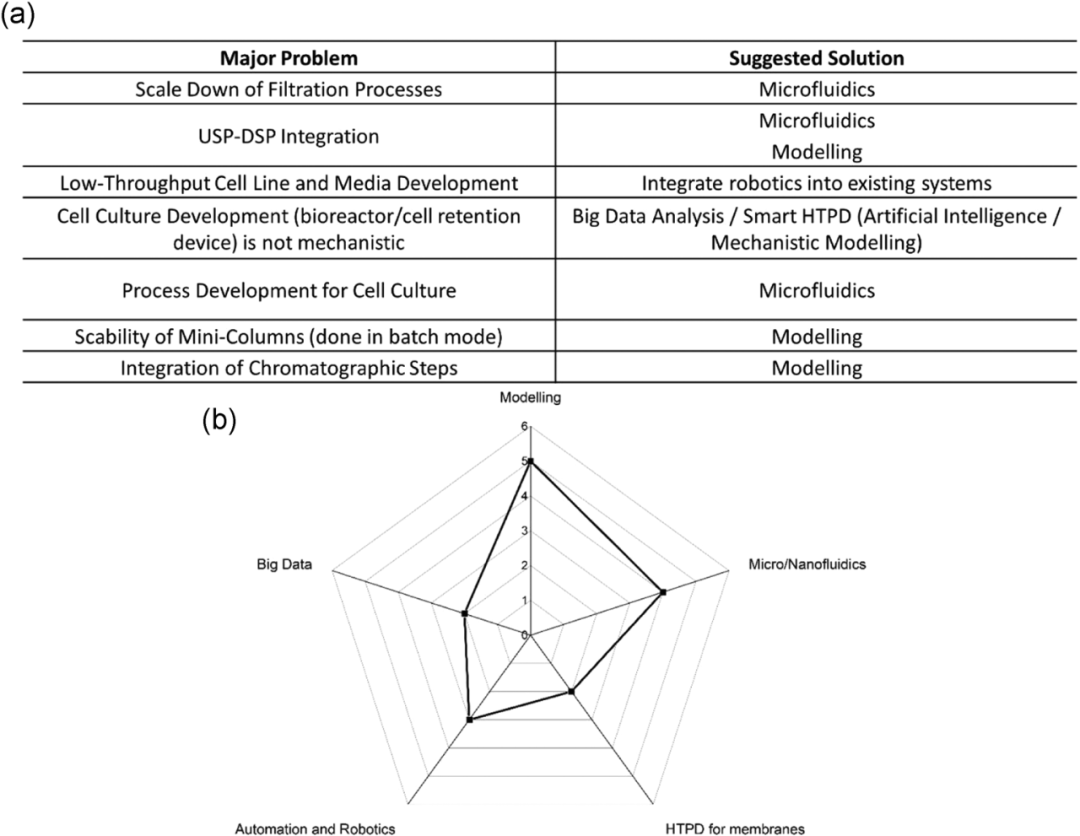
表 2 (a) 研討會參與者指出的主要問題,以及針對 ICB 工藝開發投資/優先考慮的建議解決方案/領域;(b)參與者建議的工具摘要(只有六個小組回答了這個問題)作為 ICB 中 HTPD 當前差距/問題的解決方案
過程分析技術
PAT 被定義為“通過及時測量(即在工藝過程中)原材料和過程中材料和工藝關鍵質量和性能屬性來設計、分析和控制生產的系統,以確保最終產品質量”。在生物制藥行業實施 PAT 的最終目標是設計和開發易于理解的工藝,通過實時監控原材料或過程中的產品屬性來控制工藝,從而可靠地確保最終產品的預定質量,即關鍵質量屬性(CQA)。PAT 框架提供的、清晰的過程控制和理解支持生物制藥行業采用質量源于設計 (QbD) 方法。QbD 被定義為“基于健全的科學和質量風險管理,以預先確定的目標開始,并強調對產品和工藝的理解以及過程控制的系統開發方法”。因此,PAT 實施將有助于這種系統化的工藝開發方法,通過提供對產品和工藝設計的更好理解,確保一致的產品質量。
PAT 應用在連續工藝中的關鍵要素是能夠收集 CQA 信息并觸發及時響應,以促進控制。分析測量必須在促進實時決策所需的時間范圍內可用。此外,為了輕松實施 PAT 工具,儀器所需的成本不應該很高,至少在它不會大幅增加生物制藥生產成本之前是這樣。此外,選擇的分析技術必須精確、準確和穩健。雖然連續工藝可從 PAT 實施中獲得很多收益,但這些類型的工具還沒有被充分探索過,并且針對連續工藝的發展,傳感器技術、配置和穩健性仍需要重大改進。
關于上游工藝,經典過程傳感器提供有關工藝變量的信息,例如溫度、pH、溶解氣體和泡沫水平。然而,涉及光譜傳感器的、更強大的技術已成功用于過程監控。例如,近紅外光譜已被最廣泛地研究,以用于確定細胞培養液中單個成分的濃度,如 Arnold 等人所證明的那樣。此外,拉曼光譜不僅可用于分析培養液成分譜,還可以用于監測蛋白質的結構/化學變化,尤其是用于在線監測聚體形成或糖基化等質量屬性。最近,基于液相色譜-質譜的多屬性方法已成為一種重要的 PAT,允許同時監測產品質量屬性,如聚糖譜、電荷異構體和生物治療藥物的純度。通過開發一個平臺,從生物反應器中收集無細胞樣品,然后使用自動液體處理系統進行自動高通量純化,Dong 等人(2016)證明可以產生“近乎實時”的測量,為使用此類技術在整個生物生產過程中監測多個 CQA 奠定了堅實的基礎。
對于下游工藝,PAT 的實施仍然相當有限,部分原因是缺乏傳感器選項:pH、電導率、吸光度和壓力傳感器實際上并不能測量生物分子的質量屬性,例如蛋白質聚集。然而,Kamga 等人 (2013) 采用多波長紫外光譜來有效地確定蛋白質混合物中單個成分的濃度,準確預測相對于目的蛋白質的聚體濃度。此外,對于層析步驟,實施 PAT 可能具有挑戰性,因為這些單元操作的典型工藝時間很短。Sharma等人 (2006) 證明,通過在線分析型 LC,可以實現對層析步驟的連續監測,以發現聚集峰。使用在線高效液相色譜 (HPLC) 系統研究工藝層析柱的實時合并,并對其編程,以在聚集峰開始時停止收集,結果顯示,使用 PAT,可促進基于產品質量屬性的層析柱合并的實時決策。
因此,在連續工藝中,PAT 工具必須為后續的工藝步驟在線提供決定性信息,從而使工藝的連續性成為可能。未來,這些 PAT 的開發和實施將允許設計生產工藝,從而提供一致的、明確定義的優質產品并提高工藝效率。可預見的挑戰包括實施非侵入過程監測技術,以及將先進傳感器整合到自動化過程控制策略中。
數據采集/建模
生物技術行業中的生物工藝存在許多挑戰,并且通常不如其它行業那么簡單。操作的復雜性,尤其是發酵的復雜性,使該行業多年來一直處于“試錯-優化”模式。然而,近年來,隨著 QbD 和 PAT 的應用,人們對更好地理解這一工藝有了更大的推動。這使科學家和工程師能夠對每個操作擁有更多的知識和細節了解,而不是將工藝純粹視為“黑匣子”。將一個工藝(無論是發酵等相對復雜的過程,還是混合罐等更簡單的過程)轉化為數學模型的能力不僅可以加深對工藝的理解,還可以減少優化所需的時間和實驗數量。機械模型 (MM) 旨在準確描述要描述的系統的物理化學現象,并且行業已經針對生物工藝發布了幾個此類模型的示例。除了純粹的機械模型之外,使用 MM 和機器學習的混合方法(如人工神經網絡)可以幫助減輕計算機上的計算負載,例如,通過使用數據集來確定某些參數,然后將其用作模型的輸入。這加速了工藝開發并提供了更快的結果,如文獻中所示,用于估計工藝參數和優化整個下游工藝。一旦對此類模型進行了調整和訓練,這些計算的輸出將為工藝提供非常有價值的見解。很明顯,無論是在工藝開發階段還是在生產工廠中實施此類工藝后,模型對于向集成式連續生物生產的飛躍都非常重要。然而,建模不能完全脫離實驗工作和數據。它需要數據來估計參數、訓練模型并最終驗證它們。此外,數學模型對于急需的控制策略的實施和實現非常重要,這對于確保如此復雜的生產線的正常運行至關重要。
模型的使用現在被工業界廣泛接受,并且肯定是未來連續工藝的一個關鍵特征。行業需要能夠根據基于準確描述的模型對工藝的意外變化做出動態決策的能力。這也提出了對可靠和準確數據收集的需求。再加上日益改進的傳感器,非常需要快速且準確的分析,不僅收集有關工藝行為的數據,以便快速采取行動,而且能夠監測和控制 CQA,并維護最終產品質量。考慮到生產工廠中發生的所有單元操作和過程,生成的數據量可能是巨大的。盡管生成的大量數據對于工藝理解和監控至關重要,但數據分析的自動化也同樣至關重要。集成式連續生物生產倡議渴望找到方法來容納和充分利用所有生成的數據,無論是用于工藝控制、工藝概覽還是工藝開發。
上游/下游工藝連接
對于真正集成的連續生物生產,連續單元操作(上游和下游)的不間斷連接是必要的,它們之間沒有或很少發生隔離的中間性保持步驟。
行業已經建立了幾個將連續上游工藝與捕獲步驟相結合的例子,使用灌流培養技術從生物反應器中連續去除培養基和細胞外產物。整合這兩個工藝步驟的一個主要挑戰是使上游灌流流速與下游純化流速同步。上游和下游系統之間的同步控制系統目前也較缺乏。因此,下游系統(前饋控制)不會檢測到上游工藝的偏差,反之亦然(反饋控制)。這種類型的系統需要進一步的開發和測試,因為多個上游參數會影響后續的下游操作。Karst等人證明了通過安裝近線 HPLC 來實施反饋控制的可能性,以提供生物反應器收獲液的滴度數據,以調節捕獲步驟的操作條件并通過使用控制回路調節連續體積流速。
盡管連續上游生物工藝已經相當完善,但完全連續的下游工藝的整合仍然是一個待開發領域。對于連續捕獲和精純層析,可以應用兩個主要系統:周期性逆流層析 (PCC) 和模擬移動床層析。在真正集成的連續層析平臺中,可以通過調節層析柱中的保留時間超過連續的柱步驟來實現工藝同步。為確保來自一根層析柱的劣質洗脫液材料不會與下一個功能性層析柱的材料混合,需要實時監測和反饋控制。柱之間的合并也可能引入交叉污染的風險,而反饋控制策略可能能夠檢測到流出液并將流出液從第二根柱轉移。
Gomis-Fons等人(2019)在小規模條件下開發了不同層析柱和用于純化重組蛋白的超濾單元之間的連接。外部控制器 Orbit 用于使系統自動化,并應用了開環和閉環控制策略:例如,入線監測 UV,并使用基于吸光度水平的自動產品合并。此外,在集成的連續下游工藝中,耗材需求(如層析填料和緩沖液消耗)的顯著減少將導致運營成本的大幅降低。Gjoka等人 (2017) 將4個純化單元操作轉換為連續工藝,與相應的批次工藝過程相比,分別減少了 95% 和 44% 以上所需的填料和緩沖液體積,并顯著降低了耗材消耗。因此,一個完全集成的連續工藝有可能優化質量、成本、速度和靈活性,最緊迫的挑戰是為整個生物生產過程創建一個全局性的監測和控制策略。這不僅需要監測和控制所有入口和出口液流的連續測量(PAT 框架),還需要可現實的反饋和前饋控制策略,以確保最終產品質量。到目前為止,據作者所知,生產過程中的完整端到端集成仍有待開發。然而,Godawat 等人(2015) 已能夠將灌流生物反應器與兩個周期性 PCC 單元相結合,用于初始捕獲和連續的離子交換步驟,表明創建完全集成的端到端連續生物工藝平臺是可行的。最近,Coolbaugh 等人(2021)通過在中試規模上進行的成功概念證明,證明了這種端到端的連續工藝是可放大的。
其它需求
前文所述需求代表了需要進一步開發的三大領域。然而,也有一些需求完全沒有得到關注,而另一些需求盡管沒有完全被忽視,但仍然缺乏作為可靠解決方案的實用和/或可負擔的技術。高通量篩選 (HTS) 日益普及,導致世界各地的工廠采用更自動化的實驗室和小型化分析。長期以來,自動化液體處理系統的使用已被確立為 HTPD 在下游(主要是層析)中的標準,已經有報道描述了測定吸附等溫線甚至完整層析運行的方法。使用此類設備可以實現檢測的自動化,同時保持低使用量,從而實現更快、更具成本效益的分析。對于上游來說,HTPD 已經有了解決方案,但是,這些解決方案通常帶有非常高的價格標簽,例如 Ambr?系統,這可能會阻礙科學家和行業公司對此進行的投資。因此,該行業正在呼吁尋找負擔得起的替代品,并認為微流體是滿足這一需求的好機會。在細胞系開發方面,目前對于沒有 Ambr? 系統的公司來說,最先進的技術是以批次模式獲取性能更好的細胞株,然后在灌流模式下對其進行測試。因此,需要對細胞生物學有更深入的了解,這最終將推動以可承受的價格開發出更好的細胞系,而微流控技術將提供這一點。
微流控已被證明是一種強大的規模縮小模型,能夠模擬多個單元操作,其優勢在于使用更少的樣本量并實現更快的分析。這些設備仍需要為在工藝開發中的應用鋪平道路,但在結晶、層析、細胞培養、水雙相系統、生物催化等不同的單元操作中已經顯示出有希望的結果,并且已作為 HTS 設備的有希望的縮小模型。然而,過濾仍缺乏允許實現特定單元操作 HTPD 的規模縮小模型。膜過濾在微流體中也沒有廣泛使用。液體處理站對這種單元操作的 HTPD 的適應仍處于非常早期的階段。過濾工藝開發通常需要大量的材料和耗時的工作。在這樣的系統中使用 HTS 設備可減少工藝開發中的試劑消耗,同時避免設備尺寸過大,后者往往是工藝了解較差的結果。
結論
向連續工藝的轉變是成熟行業的自然路徑,生物制藥行業正在其它行業的步伐,技術進步越來越多地推動了這種轉變。這項技術的優點是巨大的,并且得到了很好的證明,即其可以在不同的規模上降低工藝成本,即使在不同的生產規模條件下,與最成熟的批次模式相比,也是如此。
通常,連續工藝允許實現更高效的工藝,同時降低占用空間。由于設備的使用效率更高,增加體積流速意味著連續工藝的設備和耗材成本的增加比批次工藝中觀察到的要小。與連續生物工藝相對應的是對快速分析和控制的需求增加,這可以對操作條件的波動提供實時響應,以保證產品質量。
盡管過去 20 年的技術突破是巨大的,但我們可以理解,學術界和工業界都渴望更好的工藝技術。從研討會的結果可以得出結論,雖然工藝開發和優化有很多選擇,但改進的空間仍然很大,要么擁有新技術,要么找到降低現有技術價格的方法,以使工藝開發“民主化”。被認為最有希望填補 ICB 當前空白的工具包括建模和微/納米流體。這符合監管機構在 PAT 和 QbD 倡議中的當前要求,其中更高的過程理解是為了實現對最終產品質量的控制,從而降低產品差異,滿足CQA。
上游和下游工藝研究的最新進展允許實現以連續模式運行具有競爭力的單元操作,從而使這些新工藝優于先前建立的工藝。由于多年來上游和下游工藝是分開開發的,現在的挑戰在于將所有這些單元操作集成到一個連續的端到端生產過程中。軟件和硬件的集成對于實現完全連續的工藝流程以及前饋和反饋的工藝控制非常重要,以便根據其它單元操作中發生的情況做出更快的決策。PAT 的進一步發展和控制系統的同步化將是生物制藥行業向端到端連續工藝轉變的關鍵推動力。
縮短上市時間通常會阻礙連續工藝的實施,因為更容易“安全行事”并確保“贏得比賽”。然而,生物仿制藥可以利用專利到期并押注這種工藝模式,旨在實現更高效、更便宜的工藝,使生物仿制藥生產公司能夠與其它參與者競爭。
原文:M.N.Sao Pedro, T.C.Silva, R.Patil, et al., White paper on high‐throughput process development for integrated continuous biomanufacturing. Biotechnology and Bioengineering, 2021, DOI: 10.1002/bit.27757.






