本文節選自來自AGC Inc., 的研究人員發表的文章“CDMOs Play a Critical Role in the Biopharmaceutical Ecosystem”,由于水平有限,詳細內容,請參考原文。
千禧年后,生物制藥行業取得了顯著進步。新型生物藥相繼研發,重磅藥物相繼問世。伴隨著生物制藥需求的增加,出現了一種稱為“合同開發和制造組織(CDMO)”的商業模式。 CDMO 受托開發和生產制藥公司的生產工藝。在這篇綜述中,我們通過分析半導體行業的代工業務,確定生物制藥 CDMO 的成功因素。此外,我們還將回顧單克隆抗體生產平臺和新技術,它們是生物制藥 CDMO 差異化戰略的關鍵方面。
簡介
生物制藥藥物或生物制品是使用生物技術生產的藥物的總稱。與化學生產的小分子藥物不同,生物制品是復雜的分子,例如用作藥物成分的蛋白質或細胞。蛋白質療法在 20 世紀是一個小眾市場,但隨著 21 世紀抗體藥物的出現,它發生了翻天覆地的變化。最終,蛋白質療法主導了制藥行業新藥的銷售,導致范式轉變。 2012 年生物制品在前 100 名藥品總銷售額中的份額超過 16%,預計到 2026 年將達到 55%。全球處方藥中生物制品的銷售額繼續快速增長,2019 年至 2026 年的年均增長率為 9.6%。此外,已經開發出新的方式,例如基因治療藥物,來治療未滿足的醫療需求。
在生物制藥行業取得顯著進步的同時,與生物制藥公司簽訂合同進行原料藥開發和生產的合同開發和制造組織 (CDMO) 也在同步發展。圖 1 顯示了制藥行業的生態系統,它是生物技術和制藥公司的藥物發現以及 CDMO 的藥物生產的橫向劃分模型。 2018年生物醫藥CDMO產業市場規模突破100億美元,加上抗體藥物的不斷發展,各種新型生物藥不斷涌現,擴大了生物醫藥CDMO市場。預計 2020 年至 2025 年年均增長率為 10.2%,高于小分子藥物市場(8.0%)。
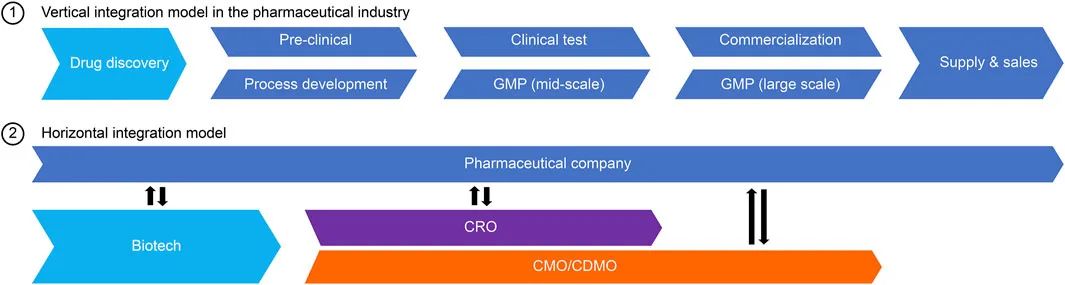
圖 1. 制藥行業的橫向角色劃分。
在生物制藥行業之前,半導體行業在80年代就建立了橫向分工模式。半導體生態系統分為以下三個部分:無晶圓廠、為其他公司生產微芯片的代工廠和集成設備生產商 (IDM)。圖2是醫藥行業和半導體行業的橫向商業模式對比。在這個模型中,半導體公司和無晶圓廠公司的設計部門的職位分別對應于制藥公司和藥物發現初創公司的藥物發現部門。盡管每個行業的產品各不相同,但兩個行業都承受著新產品和生產技術研發成本增加的負擔。半導體行業的發展和技術平臺的歷史為生物制藥 CDMO 行業的關鍵成功因素提供了見解。
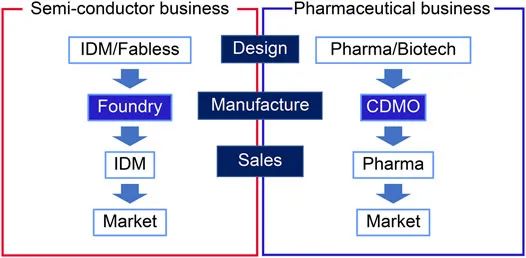
圖 2. 半導體和制藥行業的比較。
半導體代工成長背景
半導體行業的歷史背景對晶圓代工廠的成長有著重大影響。在晶圓代工興起之前,無晶圓廠公司將生產外包給 IDM。然而,無晶圓廠的發展受制于生產能力和IDM缺乏必要的生產技術。 20世紀80年代,許多無晶圓廠公司隨著晶圓代工公司的成立,開始進軍半導體業務。這些無晶圓廠公司為半導體芯片的創新做出了重大貢獻。在 2000 年代,無晶圓廠公司和其他公司,如谷歌和亞馬遜,開始設計專用芯片,并將芯片生產外包給代工廠。由于對半導體生產的需求不斷增加,晶圓代工市場在 2018 年達到 736 億美元,到 2022 年將達到 1512 億美元。預計到 2025 年復合年增長率將達到 11.6%。
半導體代工廠的成功因素
代工廠的關鍵成功因素之一是及時確保高質量和高性能半導體產品的供應。隨著半導體市場的增長,代工廠需要大量投資,以確保其產能。盡管如此,IDM在生產設備方面也需要大量資金投入,但設備的開工率取決于其新產品的銷售情況。因此,運營比率的下降可能是一種管理風險。相比之下,由于晶圓代工廠可以同時接到IDM和無晶圓廠公司的代工訂單,因此可以保持生產設備的高運轉率。因此,無晶圓廠公司可以專注于設計,代工廠可以專注于確保生產工藝能力。目前,幾家實力雄厚的晶圓代工廠在半導體行業處于領先地位。然而,IDM、無晶圓廠和代工廠的共存對于半導體行業的發展將是必要的。
獲得新技術是另一個成功因素。微細加工是半導體生產過程中最關鍵的技術之一。在半導體行業,器件的小型化按照摩爾定律進行(半導體集成率在 18-24 個月內翻一番)。這種微細加工的發展使得增加每單位面積的晶體管數量成為可能,顯著有助于提高運行速度和降低功耗。已經發明了先進的工藝技術,例如極紫外 (EUV) 光,以克服使用紫外光的傳統曝光設備的微加工限制。近年來,一流的晶圓代工廠迅速引入這些微細加工技術,并發展出基于最新設計規則的芯片生產能力。因此,對具有高生產技術的代工廠的依賴正在增加。
生物制藥合同開發和制造組織(CDMO)的成長背景
制藥公司還需要將其投資和資源集中用于新藥發現。大型制藥公司的總研發成本(2006-2014 年)在 10-900 億美元之間,新藥上市數量往往與研發成本成正比。因此,制藥公司(相當于半導體行業的 IDM)越來越難以投資于工藝開發和生產,并開始依賴 CDMO(相當于半導體行業的代工廠)。此外,由于生物技術的發展,藥物發現生物技術(相當于半導體行業的無晶圓廠)開發了許多針對各種罕見疾病的創新模式。生物技術公司和中小型制藥公司越來越多地將生產外包,以避免投資生產設施的風險。
生物制品合同開發和制造組織的成功因素
通過比較半導體代工廠和生物制品合同業務,我們發現他們成功的幾個重要共同因素如下:
1)采用先進技術保障生產技術。
2) 確保及時的設備能力。
3) 根據客戶要求提供適當的服務。
在半導體行業,隨著生產設備的發展,生產技術已經標準化,使得半導體生產外包成為可能。因此,無晶圓廠公司與代工廠合作發展壯大。此外,隨著微細加工技術的發展,半導體生產技術取得了顯著進步,僅通過購買設備很難創造出產品。代工廠擁有先進的生產技術,結合了復雜的工藝和操作訣竅。在生物制藥行業,生物制品,特別是抗體藥物,的生產已經標準化。這種標準化使得將生物制藥藥物的生產外包給 CDMO 變得更加容易。在此背景下,生物制藥CDMO的進一步發展將取決于其生產技術的進步。在下一節中,我們將回顧作為主流生物制品的抗體藥物的生產技術趨勢。我們還將討論下一代生物制品生產系統的潛力。
抗體藥物生產標準化技術助推生物制藥合同開發和制造組織業務
抗體是免疫系統用來識別和中和稱為抗原的異物的蛋白質。利用結合各種靶分子的能力,許多抗體藥物已被開發并投放市場。抗體由兩條多肽鏈組成,一條重鏈(H)和一條輕鏈(L),每條多肽鏈又由兩個區域組成,一個恒定區(C)和一個可變區(V)。可變區的互補決定區 (CDR) 對于抗體與其預期靶標結合的能力至關重要。大多數抗體藥物是將小鼠單克隆抗體的CDR移植到人源抗體中構建的人源化抗體,表明抗體藥物具有幾乎相同的理化性質。因此,可以使抗體藥物的生產過程標準化。抗體藥物生產平臺的一般流程由上游和下游工藝組成。上游工藝包括生產細胞系和在生物反應器中培養細胞系的過程,下游工藝包括從培養基中純化產生的抗體成分、滅活病毒并將其作為藥物物質灌裝的過程。大多數工藝是批次式的,并由制藥廠的良好生產規范 (GMP) 生產過程控制。由于抗體生產過程的標準化,導致生產設備、周邊輔助材料、原料系統的標準化。抗體生產的標準化使生物制藥公司更容易將其生產外包給生物制藥 CDMO。
如上一章所述,半導體行業的晶圓廠通過獲取新技術和積累半導體器件生產的可靠記錄,確立了半導體生產技術等于或優于 IDM 的地位。我們相信生物制藥CDMO可以提供與制藥公司同等質量的生產技術。為了在半導體行業建立與晶圓代工類似的地位,生物制藥 CDMO 獲取和開發獨特的生產技術將非常重要。在接下來的章節中,我們將回顧抗體藥物生產技術的最新趨勢,同時展示生物制藥 CDMO 先進技術發展的例子。
細胞系開發過程
各種細胞系已被用于生產抗體藥物,但當今最常用的細胞系是中國倉鼠卵巢 (CHO) 細胞。盡管 CHO 細胞除抗體藥物外還被用于生產各種蛋白質治療藥物,但就高生產率、糖基化質量和安全性而言,它們是抗體藥物最相容的生產細胞。下文描述了 CDMO 對 CHO 細胞進行研究和開發的示例。
為了大規模生產治療性蛋白質,包括單克隆抗體 (mAb),使用基于二氫葉酸還原酶 (DHFR) 的甲氨蝶呤 (MTX) 選擇建立重組中國倉鼠卵巢 (rCHO) 細胞。然而,它需要多輪 MTX 選擇,以進行逐步基因擴增,從而導致細胞系生成的時間線更長。 LONZA(瑞士)開發了CHO-GS(谷胱甘肽合成酶)系統來解決這個問題。在 CHO-GS 系統中,高產細胞系的選擇基于控制 GS 表達水平與其特異性抑制劑 l-甲硫氨酸亞砜亞胺 (MSX) 濃度之間的平衡。 CHO-GS 系統吸引了從風險投資公司到大型制藥公司的廣泛客戶,因為它只需要一輪 MSX 選擇。最近,LONZA 與輝瑞合作開發了一種通過同源重組位點特異性引入抗體基因的方法。與抗體基因隨機插入基因組的傳統方法相比,該方法制備的細胞可提供穩定的抗體表達水平。 AGC Biologics(美國)還開發了一種 CHEF1 系統,該系統使用 EF-1 α 啟動子顯著提高了重組蛋白的生產率。 AGC Biologics 進一步開發了一種具有更高抗體生產率的系統,其中選擇標記(二氫葉酸還原酶)基因的 DNA 密碼子被修飾,以抑制表達,以擴增細胞中引入的質粒基因。
作為最近的趨勢,值得注意的是,通過組學分析對代謝途徑進行綜合分析對于細胞系開發至關重要。例如,對典型CHO細胞親本株(CHO-K1、CHO-DXB11和CHO-DG44)的系統分析表明,抗體的糖鏈結構差異是由于所涉及的各種基因表達水平的差異。組學分析也是優化培養基成分的強大工具。Ali等人闡明了培養基中缺乏半胱氨酸是如何降低抗體生產率的。轉錄組和蛋白質組的分析導致闡明了各種因素(例如內質網應激)影響抗體產生的機制。組學分析方法是提高生產的有效方法。此外,通過基因組編輯技術(例如 CRISPR/Cas9)提高 CHO 細胞抗體生產力的試驗正在增加。
培養和純化工藝
2000 年代初期,大規模生產暢銷藥物是生物制藥 CDMO 行業的主流。然而,近年來,罕見病等生物制品的管線增加,這有利于品種更廣、數量更少的生產方案。因此,對高度靈活的一次性反應器的需求增加了。一次性系統是由塑料制成的可拋棄型設備,主要用于生物生產的上游工藝。因為每批生產都是用新的一次性設備準備的,所以不需要清潔和伴隨的驗證工作。因此,可以比不銹鋼生物反應器更快地開始生產。事實證明,一次性反應器和不銹鋼反應器之間的產品質量沒有差異。
高密度培養或連續培養方法作為上游工藝中降低資本成本和提高生產率的另一種技術引起了人們的關注。連續生產允許在小型設施中進行大量培養。此外,通過連續置換培養基,可以將乳酸或氨等代謝物的濃度保持在較低水平,從而延長細胞的壽命。連續培養可以提高產品質量。與補料分批工藝相比,灌流工藝產生的雙特異性抗體聚體明顯減少。
通過細胞工程和培養工藝的優化,抗體生產率已顯著提高至約 10 g/L 培養物。因此,下游工藝得到了優化。抗體純化的第一步一般是使用Protein A 的親和層析,它與抗體的恒定區結合。該步驟需要大量昂貴的Protein A 填料,從而提高了生產成本。連續層析法因解決這一問題而受到關注。有研究開發了連續逆流切向層析法 (CCTC),它可以用較少量的填料有效地純化抗體。在該方法中,Protein A填料循環流動,不斷吸附和解吸抗體;因此,所需的填料用量比批次法少約3倍,而CCTC法純化抗體的產品質量(HCP、DNA、單分子量餾分)與批次法相當。盡管已經報道了替代填料的開發,但它們是否可以在抗體藥物的生產中替代Protein A 填料仍不確定。
下一代生產工藝
端到端的連續生產工藝作為未來有利的生物制品生產系統而備受關注。圖 3 描述了使用 (I) 灌流生物反應器、(II) 多柱層析捕獲、(III) 病毒滅活、(IV) 膜層析精純、(V) 濃縮和緩沖液置換以及(VI) 保存過程。連續工藝不需要為每個工藝步驟提取產品,這可以減少生產的總時間和操作員數量以及人為錯誤和污染的風險。此外,通過實時監控質量,可以實現高度可靠的質量保證。一些成本模擬表明,抗體藥物的生產成本將通過持續生產而降低。雖然連續生產工藝生產各種小分子藥物,但生物制品的連續生產仍在開發中。已經報道了實驗室規模的抗體藥物的完整連續生產工藝。使用該方法,成功連續培養 18 天,與批次法相比,產品質量可以接受。
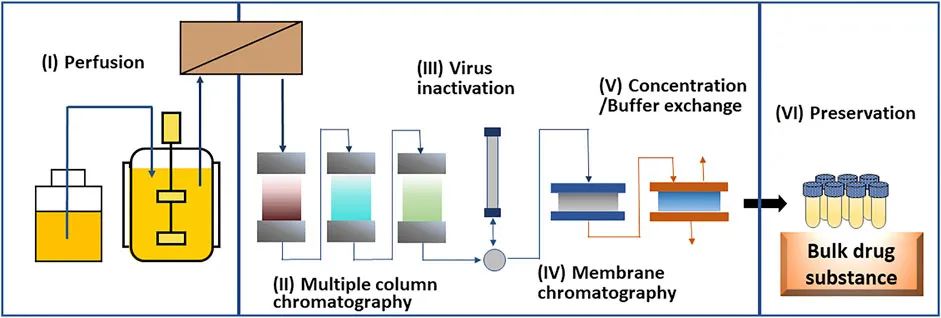
圖 3. 治療性單克隆抗體的端到端連續生產工藝過程示意圖。
盡管有上面討論的優點,但迄今為止在實施連續生產方面的進展似乎比預期的要慢。這主要是因為連續工藝的開發和實施需要很長時間才能收回初始投資。Badman等人提出了一些有趣的想法,例如稅收和監管激勵措施,以促進從批次工藝系統到連續系統的過渡。由于系統的高度復雜性,連續生產方法的使用也受到限制。盡管監控和數據采集 (SCADA) 等數字技術也得到了發展,但要在實際環境中實現生物制品的端到端連續生產,仍有改進的空間。過程分析技術 (PAT) 已在批次或補料分批操作中得到發展。我們相信,PAT 與數字數據管理系統相結合的進一步發展也將有助于向生物制藥行業的連續生產過渡。
結論
在生物制藥行業,在藥物發現和生產過程中都發生了許多技術創新。與此同時,醫藥行業的橫向分工模式也變得必不可少;生物制藥公司(和生物技術公司)更專注于藥物發現和開發,而 CDMO 更專注于工藝開發和生產。生物制藥 CDMO 可以向半導體行業學習,其中代工廠建立了類似于 IDM 的技術地位。 CDMO 加大技術開發投資和獲取新技術以保持競爭優勢將更為關鍵。我們相信,通過持續支持生物制藥行業生產針對更多疾病的生物藥物,CDMO 將為健康生活做出重大貢獻。
原文:H.Kurata, T.Ishino, Y.Ohshima, et al., CDMOs Play a Critical Role in the Biopharmaceutical Ecosystem. Front. Bioeng. Biotechnol., 2022.






